Zakład Farmakologii Bólu
Profil naukowy
- O zakładzie
- Pracownicy
Opis zakładu
Tematyką badawczą Zakładu Farmakologii Bólu jest opracowywanie zagadnień dotyczących problematyki powstawania i utrzymywania się procesów bólowych, ze szczególnym uwzględnieniem bólu neuropatycznego, który powstaje w wyniku uszkodzenia nerwów obwodowych z powodu urazów, nowotworów, cukrzycy, stwardnienia rozsianego, niedotlenienia. Ten rodzaj bólu nie jest łagodzony przez typowe środki przeciwbólowe, dlatego też staje się często dolegliwością bez perspektyw na znaczną poprawę. Pomimo licznych badań zarówno klinicznych jak i doświadczalnych, molekularny mechanizm rozwoju bólu wciąż nie jest dokładnie poznany.
W badaniach pragniemy określić zaburzenia homeostazy w endogennych układach opioidowych, co wydaje się jedną z głównych przyczyn rozwoju bólu przewlekłego. Wzrost aktywacji endogennych systemów przeciwbólowych w odpowiedzi na uszkodzenie układu nerwowego uruchamia mechanizmy homeostazy i w konsekwencji prowadzi do nadmiernej aktywności systemów probólowych. Badania mają na celu określenie ścieżek udziału różnych probólowych peptydów w rozwoju neuropatii.
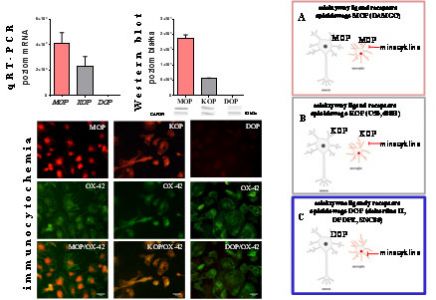
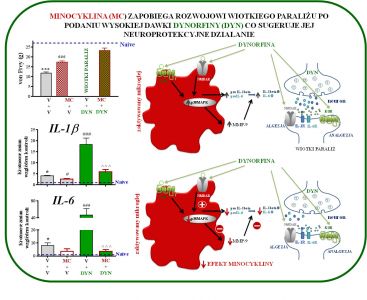
Badania z wykorzystaniem zarówno profilowania ekspresji genów jak i analizy białek wskazują, że w bólu neuropatycznym dochodzi do silnej aktywacji wielu genów neuronalnych, jak również genów związanych z odpowiedzią komórek immunologicznych, w tym z aktywacją mikrogleju. Prowadzone badania są istotne, ponieważ obecnie brak danych dotyczących prób hamowania mikrogleju czy czynników prozapalnych takich jak IL-1beta, CCL2, CCL5, a także wykorzystania inhibitorów szlaków wewnątrzkomórkowych NF-B, ERK1/2, p38MAPK przy stosowaniu opioidów w bólu neuropatycznym. W badaniach poszukujemy nowych punktów uchwytu również dla skutecznej terapii neuropatii cukrzycowej. Prowadzone eksperymenty wykazały, że modulacja zmian neuroimmunologicznych na skutek działania pentoksyfiliny (inhibitor pozapalnych cytokin), minocykliny (inhibitor p38MAPK), partenolidu (inhibitor NF-κB), U0126 (inhibitor ERK1/2), SB203580 (inhibitor p38MAPK) PD98059 (inhibitor MAPKK) w bólu neuropatycznym osłabia jego rozwój a także nasila efektywność opioidów. Mamy nadzieję, że wyniki naszych badań stworzą eksperymentalne podstawy do zastosowanie w przyszłości skojarzonej terapii stosowanych w klinice opioidowych leków przeciwbólowych z inhibitorami gleju lub innymi substancjami modulującymi syntezę lub działanie prozapalnych czynników, w celu zwiększenia skuteczności leków przeciwbólowych w terapii bólu neuropatycznego.
Metody badawcze




Pracownicy zakładu
prof. dr hab. Barbara Przewłocka
dr Anna Piotrowska-Murzyn
dr hab. Ewelina Rojewska-Mendel
dr Agata Ciechanowska
mgr Wioletta Makuch
mgr Aleksandra Bober
mgr Katarzyna Ciapała
Agnieszka Młynarczyk
mgr inż. Katarzyna Pawlik-Szczerba
Dokonania naukowe
- Publikacje
- Granty
Grant
PRELUDIUM 12 2016/23/N/NZ7/00356 Określenie mechanizmów i potencjalnych punktów uchwytu dla terapii bólu neuropatycznego poprzez zbadanie interakcji farmakologicznych pomiędzy substancjami modulującymi aktywność gleju a lekami opioidowymi
Dr Anna Piotrowska-Murzyn
Grant
OPUS 22 2021/43/B/NZ7/00230 Nowe strategie w farmakoterapii bólu neuropatycznego oparte na modulacji układu chemokin i jego wpływie na rozwój tolerancji opioidowej
prof. dr hab. Joanna Mika
Analgesic Properties of Opioid/NK1 Multitarget Ligands with Distinct in Vitro Profiles in Naive and Chronic Constriction Injury Mice
Starnowska, J., Costante, R., Guillemyn, K., Popiolek-Barczyk, K., Chung, N.N., Lemieux, C., Keresztes, A., Van Duppen, J., Mollica, A., Streicher, J., Vanden Broeck, J., Schiller, P.W., Tourwé, D., Mika, J., Ballet, S., Przewlocka, B.
DOI: 10.1021/acschemneuro.7b00226
The multiplicity of spinal AA-5-HT anti-nociceptive action in a rat model of neuropathic pain
Malek, N., Kostrzewa, M., Makuch, W., Pajak, A., Kucharczyk, M., Piscitelli, F., Przewlocka, B., Di Marzo, V., Starowicz, K.
DOI: 10.1016/j.phrs.2016.06.012
Blockade of IL-18 signaling diminished neuropathic pain and enhanced the efficacy of morphine and buprenorphine
Pilat, D., Piotrowska, A., Rojewska, E., Jurga, A., Ślusarczyk, J., Makuch, W., Basta-Kaim, A., Przewlocka, B., Mika, J.
DOI: 10.1016/j.mcn.2015.12.013
Blockade of toll-like receptors (TLR2, TLR4) attenuates pain and potentiates buprenorphine analgesia in a rat neuropathic pain model
Jurga, A.M., Rojewska, E., Piotrowska, A., Makuch, W., Pilat, D., Przewlocka, B., Mika, J.
DOI: 10.1155/2016/5238730
Bifunctional Peptide-Based Opioid Agonist-Nociceptin Antagonist Ligands for Dual Treatment of Acute and Neuropathic Pain
Guillemyn, K., Starnowska, J., Lagard, C., Dyniewicz, J., Rojewska, E., Mika, J., Chung, N.N., Utard, V., Kosson, P., Lipkowski, A.W., Chevillard, L., Arranz-Gibert, P., Teixidó, M., Megarbane, B., Tourwé, D., Simonin, F., Przewlocka, B., Schiller, P.W., Ballet, S.
DOI: 10.1021/acs.jmedchem.5b01976
Pharmacological kynurenine 3-monooxygenase enzyme inhibition significantly reduces neuropathic pain in a rat model
Rojewska, E., Piotrowska, A., Makuch, W., Przewlocka, B., Mika, J.
DOI: 10.1016/j.neuropharm.2015.10.040
Participation of pro- and anti-nociceptive interleukins in botulinum toxin A-induced analgesia in a rat model of neuropathic pain
Zychowska, M., Rojewska, E., Makuch, W., Luvisetto, S., Pavone, F., Marinelli, S., Przewlocka, B., Mika, J.
DOI: 10.1016/j.ejphar.2016.09.019
Direct and indirect pharmacological modulation of CCL2/CCR2 pathway results in attenuation of neuropathic pain - In vivo and in vitro evidence
Piotrowska, A., Kwiatkowski, K., Rojewska, E., Slusarczyk, J., Makuch, W., Basta-Kaim, A., Przewlocka, B., Mika, J.
DOI: 10.1016/j.jneuroim.2016.04.017
Dataset of botulinum toxin A influence on interleukins under neuropathy
Zychowska, M., Rojewska, E., Makuch, W., Luvisetto, S., Pavone, F., Marinelli, S., Przewlocka, B., Mika, J.
DOI: 10.1016/j.dib.2016.11.023
Effects of chronic doxepin and amitriptyline administration in naïve mice and in neuropathic pain mice model
Mika, J., Jurga, A.M., Starnowska, J., Wasylewski, M., Rojewska, E., Makuch, W., Kwiatkowski, K., Malek, N., Przewlocka, B.
DOI: 10.1016/j.neuroscience.2015.03.003